中心公告
友谊消化 | 《胃肠病学》前沿速递——第65期:ENPP1调控的细胞外嘌呤代谢驱动胰腺炎介导的胰腺癌发生发展
引言
《胃肠病学》(Gastroenterology)是美国胃肠病学会(American Gastroenterology Association,AGA)的官方杂志,是国际消化病学领域的顶级学术期刊,提供了胃肠病学基础和临床研究的最新和权威报道。首都医科大学附属北京友谊医院是消化系统疾病国家临床医学研究中心和消化健康全国重点实验室依托单位,是AGA在中国唯一官方指定授权发布《胃肠病学》杂志翻译的单位。
每月两期,一起了解胃肠疾病学术前沿信息!


第65期

ENPP1调控的细胞外嘌呤代谢驱动胰腺炎介导的胰腺癌发生发展
通讯作者:
施思教授、虞先濬教授,复旦大学附属肿瘤医院胰腺外科,上海胰腺癌研究所
背景与目的:
慢性胰腺炎(CP)患者发生胰腺导管腺癌(PDAC)的风险增加。尽管已发现胰腺炎可促进PDAC的发生发展,但其如何推动胰腺癌发生的分子机制仍不清楚。本研究结合临床患者组织的多组学分析、动物模型和功能实验,解析胰腺炎向胰腺癌转化的关键通路,并评估ENPP1作为早期干预及治疗靶点的潜力。
方法:
研究首先对CP和慢性胰腺炎相关胰腺导管腺癌(CP-PDAC)患者的胰腺组织样本进行了包括代谢组、转录组以及蛋白组分析在内的多组学分析。随后构建Ptf1aCre/+;LSL-KrasG12D/+(KC)及Enpp1敲除的KCE小鼠胰腺炎-癌转化模型,并结合单细胞测序评估免疫微环境变化。进一步采用原代腺泡细胞和胰腺星状细胞(PSC)培养、3D ADM模型、受体/信号通路抑制实验以及原位移植模型,验证ENPP1-CD73-腺苷轴的功能;同时评估ENPP1抑制剂单药及联合抗PD-L1治疗的效果。
结果:
对CP和CP-PDAC患者样本进行的多组学分析表明,ENPP1调控的细胞外嘌呤代谢在胰腺炎-癌转化过程中起重要作用。从机制上看,胰腺腺泡细胞的炎症性损伤会导致嘌呤核苷酸代谢物释放,这些物质经由胰腺星状细胞表面的ENPP1-CD73复合物降解为腺苷。该过程可激活胰腺星状细胞并促进纤维化形成。活化的胰腺星状细胞随后释放CXCL17,从而在微环境中募集髓系来源的抑制性细胞和调节性T细胞,产生免疫抑制效应。最终证实ENPP1是PDAC免疫治疗的有效靶点和胰腺炎-癌转化早期干预的关键靶标。
结论:
本研究证实,ENPP1是胰腺炎介导的胰腺癌发生的重要驱动因素,有望成为胰腺炎高危人群早期干预及PDAC免疫联合治疗的重要靶点。
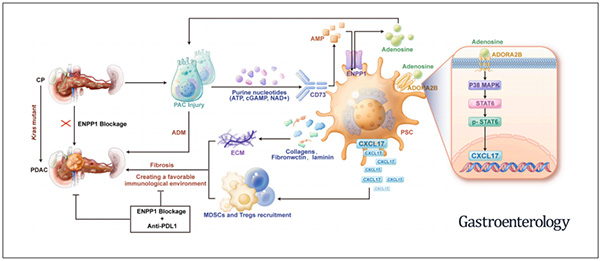
胰腺炎造成腺泡细胞损伤后,细胞外嘌呤核苷酸在PSC表面的ENPP1-CD73轴作用下转化为腺苷;腺苷再经ADORA2B-p38-STAT6通路诱导CXCL17分泌,促进PSC活化、纤维化及MDSC/Treg募集,从而驱动胰腺炎向胰腺癌转化。
图文摘要
研究亮点和启示
本研究通过对临床样本的多组学分析显示,CP-PDAC中核苷、核苷酸及其类似物显著富集,嘌呤代谢尤其是ATP-腺苷-腺嘌呤代谢轴明显上调。ENPP1和PAICS在转录和蛋白水平均持续升高,其中ENPP1高表达和较差生存相关,且主要定位于PSC/成纤维细胞群,而非胰腺癌细胞本身。在慢性胰腺炎加速致癌模型中,Enpp1缺失可明显减轻胰腺损伤、腺泡-导管化生(ADM)、纤维化及PanIN形成。纵向观察显示,KC小鼠PDAC发生率为50%,而KCE小鼠降至30%,提示ENPP1在胰腺炎向癌转化过程中具有促癌作用。
机制上,炎症损伤的腺泡细胞释放大量细胞外嘌呤核苷酸,随后在PSC表面的ENPP1-CD73轴作用下转化为腺苷。腺苷进一步通过ADORA2B-p38-STAT6信号促进CXCL17转录,驱动PSC活化和基质沉积,并招募MDSC和Treg,形成免疫抑制性微环境;同时ENPP1高表达和CD8+ T细胞减少、Treg增多密切相关。
干预实验表明,ENPP1抑制可减少ADM/PanIN病变、降低胶原沉积和PSC活化;在原位移植模型中,ENPP1抑制剂和抗PD-L1联合治疗较单药更显著抑制肿瘤生长并延长生存,提示其兼具早期预防和增强免疫治疗反应的潜力。
本研究证实,ENPP1调控的细胞外嘌呤代谢是胰腺炎促进胰腺癌发生发展的关键驱动因素。其通过“腺泡细胞损伤-ENPP1/CD73产腺苷-PSC活化-CXCL17分泌-免疫抑制”这一串联通路,加速纤维化和肿瘤进展。
本研究的突出价值在于,它并未将胰腺炎仅视为胰腺癌的“伴随背景”,而是通过人组织多组学、转基因模型和功能实验把“炎症-基质-免疫”三者连成了一条相对完整的致癌链条。研究显示,真正处于这一链条中枢位置的并不是肿瘤细胞本身,而是被腺苷重新编程后的PSC。也就是说,胰腺炎相关胰腺癌的形成,既是上皮细胞恶变的问题,也是基质代谢和免疫微环境被持续塑造的结果。
从机制创新上看,作者把ENPP1这一经典胞外核苷酸代谢酶,同ADORA2B-p38-STAT6-CXCL17通路及MDSC/Treg募集联系起来,解释了为什么胰腺炎背景下会同时出现显著纤维化和免疫抑制。这一发现提示,胰腺癌的促癌微环境并非单纯由胶原沉积构成,而是由代谢产物、基质细胞和免疫细胞共同建立的“放大回路”。因此,针对PSC激活和腺苷信号的干预,可能比单纯抑制肿瘤细胞增殖更适合用于高危阶段的早期阻断。
从临床转化角度看,ENPP1抑制既可在胰腺炎-癌转化阶段减少ADM/PanIN和纤维化,又可能在已形成的PDAC中增强抗PD-L1治疗效果,因此兼具预防和治疗双重意义。不过,作者也明确指出,目前ENPP1抑制剂的安全性和有效性仍缺乏临床试验证据,后续仍需在更大样本、更多中心和更异质的人群中验证。
译者简介
译者:张鹤扬

首都医科大学附属北京友谊医院消化科医师,中国抗癌协会肿瘤营养专委会副秘书长,中国抗癌协会肿瘤营养新苗委员会青年委员,欧洲临床营养与代谢学会(ESPEN)青年委员,Clinical Nutrition ESPEN 杂志副主编。主持国家自然科学基金青年项目1项。以第一作者身份在 Nature Communications、Advanced Science、Journal of Neuroinflammation、Journal of Cachexia, Sarcopenia and Muscle 等期刊发表SCI论著14篇,累计影响因子超100分,单篇最高引用179次,参与发明专利7项。
主要研究方向:消化系统疾病的发病机制及精准诊疗。
审核:施海韵

医学博士,首都医科大学附属北京友谊医院消化内科主任医师,副教授,青年博导。中华医学会消化病学分会胃肠微生态学组委员,中华医学会消化内镜学分会小肠镜和胶囊镜学组委员,北京整合医学学会炎症性肠病分会副主任委员,北京医学会消化病学分会肠道疾病专业副召集人,北京医学会消化病学分会青年论坛副召集人。入选北京市优秀青年人才、北京市科技新星计划等多项人才计划。主持国家自然科学基金、首都临床特色应用研究等多项科研课题。在国际、国内学术期刊发表论文30余篇,多次在DDW、APDW等国际国内学术会议做汇报交流并获青年研究者奖。主要研究方向:炎症性肠病、结直肠肿瘤与肠道微生态。
总审核:张澍田

首都医科大学附属北京友谊医院院长,消化健康全国重点实验室主任,消化系统疾病国家临床医学研究中心主任,国家临床医学协同研究创新联盟秘书长,中国医院协会第三、四届副会长,中华医学会消化内镜学分会第七届主任委员,中华医学会消化病学分会第九届副主任委员,北京医学会消化内镜学分会第六届主任委员,北京医学会消化病学分会第十届主任委员,中国医师协会消化医师分会第四、五届会长,亚太消化内镜学会第六、七届委员,世界华人消化医师协会第一届会长,中华消化内镜杂志主编,中华消化杂志副主编,中华医学杂志(英文版)副主编。
首都医科大学附属北京友谊医院消化中心简介

首都医科大学附属北京友谊医院消化中心以食管、胃肠及肝胆胰腺疾病的内镜介入(微微创)诊断与治疗为特色,国内领先、国际知名。是消化健康全国重点实验室、消化系统疾病国家临床医学研究中心、国家重点临床专科、北京市消化疾病中心。由消化一、二、三科、消化内镜中心(全球20家最卓越之一)、消化实验室和消化六科组成。目前职工总人数329人:医生106人,护理151人,科研人员32人,工程师1人,医辅人员39人;在读研究生99人。现有病床150张,消化内镜中心总面积5400平方米,共有46个操作台,其中ERCP6台。实验室总面积6000平方米。
西城院区:位于首都核心区(前门南、天坛西)
通州院区:位于北京城市副中心
顺义院区:位于首都机场附近的后沙峪



